La recherche clinique, c’est quoi?
La recherche clinique est une étape clé dans le développement de nouvelles thérapeutiques, ainsi que dans la compréhension et le diagnostic d’une maladie. 3 types d’études correspondent à ces objectifs, avec des prises en charge adaptées :
- Etudes à but thérapeutique : pour trouver un nouveau médicament
- Etudes de recherche fondamentale : pour mieux comprendre la maladie
- Etudes à but diagnostique : pour trouver de nouveaux marqueurs de la maladie.
C’est notamment au vu des résultats des études cliniques que les autorités publiques de santé autoriseront, ou non, la commercialisation d’un nouveau médicament. Chacun d’entre nous est donc potentiellement concerné par la recherche clinique.
Les étapes de la recherche clinique
La recherche clinique sur une molécule se compose de quatre phases :
- Phase I : On teste l’évolution du produit dans l’organisme en fonction du temps (pharmacocinétique) ainsi que la toxicité sur l’être humain
- Phase II : On teste la toxicité et les effets secondaires de la molécule sur un petit nombre de personnes. On cherche la dose minimale ayant une action thérapeutique et la dose maximale non toxique sur l’être humain.
- Phase III : L’expérimentation de l’essai clinique est étendue à un nombre élevé d’individu. On compare l’activité de la molécule testée par rapport à un placebo. Si les résultats de cette phase sont positifs, le produit obtiendra son autorisation de mise sur le marché par l’ANSM (AMM).
- Phase IV : Il s’agit des études pratiquées après la commercialisation du médicament. Cette phase de contrôle permet de suivre les effets secondaires des médicaments, sur une population plus large de patients et dans des conditions normales d’utilisation.
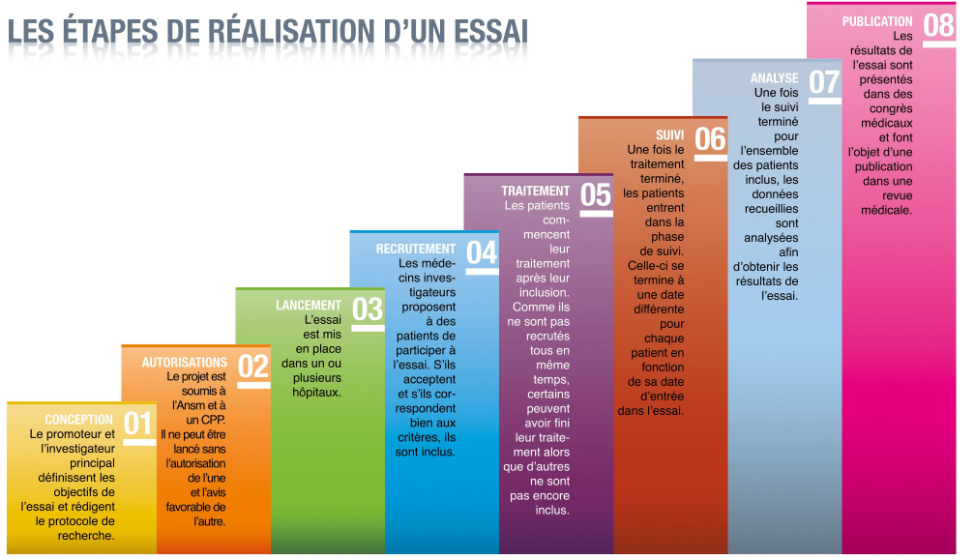
Comment se déroule un essai clinique?
- La conception : c’est le moment où le promoteur et l’investigateur principal définissent les objectifs de l’essai et rédigent le protocole.
- Les autorisations : le promoteur adresse le protocole à l’ANSM et à un CPP afin d’obtenir l’autorisation de la première et l’avis favorable du second.
- Le lancement de l’essai : le promoteur contacte des centres hospitaliers et des médecins susceptibles de participer à l’essai. En cas d’accord, la logistique nécessaire à la réalisation de l’essai est mise en place dans chacun des centres investigateurs.
- L’inclusion : c’est la période pendant laquelle chacun des médecins investigateurs sélectionne des patients parmi ceux qu’ils suivent et leur proposent d’entrer dans l’essai.
- La phase de traitement : durant cette phase, les patients inclus reçoivent le traitement prévu par le protocole.
- La phase de suivi : une fois le traitement prévu terminé, les patients sont généralement suivis pendant une période plus ou moins longue.
- L’analyse : l’ensemble des données recueillies pendant les phases de traitement et de suivi est analysé afin d’apporter la réponse à la question posée par l’essai.
- La publication : les résultats de l’essai font l’objet d’une publication dans une revue médicale afin d’être partagée avec l’ensemble de la communauté médicale.